
重庆康德2021年秋高二(上)期末联合检测试卷化学答案,目前答案易对网已经整理了重庆康德2021年秋高二(上)期末联合检测试卷化学答案的各科答案和试卷,更多联考试卷请关注本网站。


11.B由题图可知,H2O生成H2,H的化合价降低,得电子,故正极的电极反应式为2H2O 2e=H2↑ 2OH,A项错误。反应生成的OH、S-与Fe2可生成Fe(OH)2FeS,B项正确。根据题中所给信息可知,SOξ-与H2反应生成S2-,根据元素守恒可知厌氧细菌生成物中还有H2O,故反应式为4H2 SO2-十4H2O,C项错误。钢管表面镀锌,锌会与铁形成原电池,锌比铁活泼,铁作正极,可减缓钢管的腐蚀;钢管表面镀铜,铜会与铁形成原电池,铁比铜活泼,铁作负极,从而加速钢管的腐蚀,D项错误。
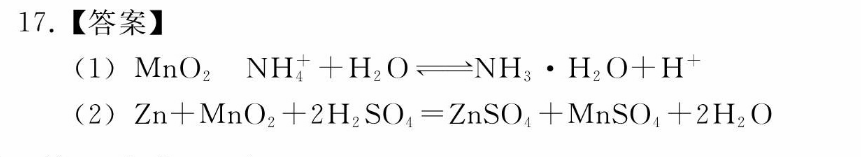

17.【答案】(1)MnO2NH4 H2O、NH3·H2O H(2) Zn MnO, 2H,SO,=ZnSO, MnSO, 2H, O(3)CH4-8e- 10OH=CO3- 7H2O(4)减小Zn2 Mn2 2H2O=Zn MnO2 4H【解析】(1)普通锌锰干电池的构造:外壳为锌筒,中间是石墨棒,其周围是由MnO2和NHCl等组成的糊状填充物,还原剂锌在负极失去电子被氧化,氧化剂MnO2在正极得到电子被还原,电解质氯化铵水解(NH十H2O。NH3·H2O十H)使电解液呈酸性(2)“酸浸”时首先会想到活泼金属锌与稀硫酸反应,Zn十H2SO4=ZnSO4 H2↑,结合“滤液”的溶质为znSO4和MnSO4可推知,在酸性溶液中强还原剂锌把强氧化剂MnO2还原为Mn2 :Zn MnO2 2H2SO4=ZnSO4 MnSO4 2H2O。(3)碱性燃料电池中,甲烷的氧化产物为CO3-:CH4-8e- 10CCO)3- 7H2O(4)铝电极与通甲烷的铂负极相连,作电解池的阴极,电解时溶液中的锌离子在铝电极上得到电子被还原为单质锌,Zn2 2e=Zn,阳极上是Mn2失去电子被氧化为MnO2,Mn2-2e十2HO=MnO2十4H,生成的氢离子使阳极附近溶液的pH减小。、阳极反应相加即为电解池中的总反应:Zn2 Mn2 2H2O=Zn MnO2 4H 。

 相关文章
相关文章
 栏目最新
栏目最新
 随机推荐
随机推荐 热门标签
热门标签